重曹とクエン酸を水に混ぜることの化学【実験と解説】
当サイトには広告を掲載しています

重曹とクエン酸を水に混ぜると、化学反応が起こり、二酸化炭素が生じて発泡します。自家製の炭酸水作りなどにも使われる身近な現象ですが、化学的に解説した一般向けの情報は多くありません。
そこで本記事では、重曹とクエン酸を混ぜると起こる化学反応について、一般の方に向けて解説します。実験の章では、pH指示薬を加えた状態で反応の様子を観察しました。
最初の章には、重曹とクエン酸をぴったり反応させるための混合量(2つを混ぜる割合)を自動で計算するツールも設置しています。
重曹とクエン酸を混ぜる量(割合)の自動計算ツール
重曹とクエン酸を混ぜて、ぴったりと過不足なく化学反応させるために必要な混合量(2つを混ぜる割合)を、自動で計算できるツールです。自家製の炭酸水や、炭酸風呂(入浴剤やバスボム)、自由研究などにお役立てください。
- 計算モードを選択してください。重曹の質量を基準にするか、クエン酸の質量を基準にするかを選択できます。
- 使用するクエン酸の種類を選択してください。無水と結晶(一水和物)の2種類があり、計算値がいくぶん異なってきます。
- 質量(グラム数)の数値を入力して、計算ボタンを押してください。ぴったりと反応する物質の質量が、自動で計算されます。
計算結果は、文章と化学反応式の図で出力されます。
計算モードを選択
使用するクエン酸の種類を選択
重曹とクエン酸が反応する割合一覧
重曹とクエン酸が反応する比率は、物質量比(モル比)で3:1です。この比は、あくまで物質量(mol)の比であり、重さや粉末の体積の比ではありません。
そこで、化学的計算や測定データに基づく、重曹とクエン酸をぴったり反応させるための混合比を下表にまとめます。
重さで量るならば例として、重曹1.312 g:クエン酸(無水)1.000 gの割合で反応させると、過不足なくぴったり化学反応させられます。
小さじなど、体積で量る場合の比も、独自の測定データに基づき算出しました。クエン酸(結晶)を使う場合は、目安として1:1の体積比になります。クエン酸(無水)の場合では、重曹の方がいくぶん多めに必要な場合が多いでしょう。
ただし、下の囲みに書いたとおり、体積を基準に「ぴったり」量るのは困難なので、体積比は目安としてご利用ください。
小さじなどで量る場合の体積比も示していますが、大まかな目安であり、当サイト独自の測定データを基に算出した一例に過ぎません。実際の比は、製品の粒径や固まり具合などに大きく左右されます。
粉末や顆粒を体積で量ると大きな誤差が出やすいので、正確に混ぜたい場合は重さで量る必要があります。
食品添加物として売られているクエン酸には、「クエン酸(無水)」と「クエン酸(結晶)」の2種類があります。それぞれ化学的には、「クエン酸無水物」と「クエン酸一水和物」のことです。
クエン酸一水和物の方は、クエン酸1分子あたり、1分子の水を取り込んで結晶化しています。そのため、1 molあたりの質量は、無水物と一水和物で異なります。すると、反応に要する質量の計算値も異なってきます。
2種類のクエン酸の違いについては、下記の記事で解説しています。
クエン酸の無水と結晶の違いを解説&実験【化学的には別の物質】 - カガクなキッチン
【実験】重曹とクエン酸の反応をpH指示薬を入れて観察
この③章では実験を行い、重曹とクエン酸の化学反応を観察してみます。化学の用語も少し使っていますが、原理などの詳しい解説は後の④章で行うので、まずは実験の様子を楽しんでいただければ幸いです。

実験を行う前に、水溶液中での重曹とクエン酸の反応について、④章でも解説する2つの事柄を示しておきます。
- クエン酸と重曹は1:3の物質量比(モル比)で反応する。この比を超えて重曹を加えても、クエン酸との反応は起こらない。
- クエン酸と重曹がぴったり反応すると、弱酸性を示す「炭酸」と、弱塩基性(弱アルカリ性)を示す「クエン酸ナトリウム」の混合水溶液ができる。
この2点を、実験的に裏付けてみようと思います。
では始めに、クエン酸水溶液を調製します。薬包紙に1.143 gのクエン酸(無水)を量り取りました。 量り取ったクエン酸を、適量の精製水(今回は30 mL強を使用)が入ったコニカルビーカーに加え、振り混ぜて溶かしました。
量り取ったクエン酸を、適量の精製水(今回は30 mL強を使用)が入ったコニカルビーカーに加え、振り混ぜて溶かしました。
化学反応に伴う液性の変化を見るため、pH指示薬としてBTB溶液(BTB指示薬の溶液)を用いました。
- BTB指示薬のpHによる色の変化
- pH6.0以下の酸性で黄色
- pH7前後の中性付近で緑色
- pH7.6以上の塩基性で青色
クエン酸水溶液は酸性なので、BTB溶液を加えると下の写真のように黄色になりました。
このクエン酸水溶液に、0.500 gずつ3回に分けて、合計1.500 gの重曹を加えます。これは計算上、先ほど溶かした1.143 gのクエン酸とぴったり反応する量です。
0.500 gずつの重曹を加えると3回とも、すぐに激しく発泡が起こりました。クエン酸は分子内に3つのカルボキシ基(-COOH基)を持つ、3価の酸です(3つの水素イオンH+を放出可能)。今回の実験では0.500 gの重曹を加える度に、1箇所ずつHがNaに置換されます。
合計1.500 gの重曹を加えた後の水溶液には、クエン酸三ナトリウムと炭酸が溶けています。溶液の色は黄緑色であり、pHはおそらく6.0~6.2程度でしょう。 弱塩基性を示すクエン酸ナトリウムが溶けているのに弱酸性なのは、炭酸の影響と考えられます。
弱塩基性を示すクエン酸ナトリウムが溶けているのに弱酸性なのは、炭酸の影響と考えられます。
炭酸(溶存二酸化炭素)は温度が高くなるほど溶解度が下がるため、加熱すれば炭酸を追い出せるはずです。そこで、水溶液の入ったコニカルビーカーを、熱湯を入れた大型のビーカーに入れて、途中何度かコニカルビーカーを持ち上げて振り混ぜつつ、しばらく放置しました。

途中3回ほど熱湯を交換しつつ加温を続けると、時間経過に伴い徐々に溶液の色が変化しました。下の画像に色調変化をまとめます。記載のpHは、BTB指示薬のカラーチャートとの比較で大まかな値を見積もったものです。 この変化は、炭酸が溶液中から追い出されていくほど、クエン酸ナトリウムの影響が大きくなり、液性が弱酸性から弱塩基性へと変わったためです。
この変化は、炭酸が溶液中から追い出されていくほど、クエン酸ナトリウムの影響が大きくなり、液性が弱酸性から弱塩基性へと変わったためです。
1時間10分ほど加温を続けた後、ターコイズブルーに近い、緑がかった青色の溶液になりました。
次に、この溶液に、さらに0.500 gの重曹を加えてみます。必要量の重曹を薬包紙に量り取りました。
量り取った重曹を、水溶液に加えました。すると、重曹が溶液の底に沈んでいますが、発泡は一切起こりません。
さらに溶液を振り混ぜても、一切発泡は見られず、重曹が水溶液に溶けきりました。重曹が溶けたことで、溶液のpHも上昇します。緑がかった青色だった溶液は、より青色に近づきました。 発泡が起こらないのは、合計1.500 gの重曹を加えた段階で、酸が反応し尽くして残っていないためです。
発泡が起こらないのは、合計1.500 gの重曹を加えた段階で、酸が反応し尽くして残っていないためです。
ちなみに、1.500 gの重曹を加えた後、「加熱せずに」さらに重曹を加えると、いくらか発泡します。これはクエン酸と重曹の化学反応によるものではなく、後述する化学平衡が移動したり、物理的刺激が与えられたりして、溶け込んでいた炭酸が二酸化炭素として気化するためです。
以上、「重曹とクエン酸は決まった比率で反応する」「反応後には弱酸性の炭酸と弱塩基性のクエン酸ナトリウムが生じる」といった理論と矛盾しない実験結果が得られました。
重曹とクエン酸を混ぜると起こる化学反応について解説
この章では、酸と塩基(アルカリ)の基礎知識を復習した後に、重曹とクエン酸の化学反応の要点を解説していきます。
まずは「酸と塩基(アルカリ)」の基本を復習
水溶液の性質を表す要因のひとつに「液性」があります。液性は、大きな分類としては酸性、中性、塩基性(アルカリ性)の3つがあり、pHを用いて数値化もできます。
では、水溶液の酸性やアルカリ性とは、そもそも何を表しているのでしょうか?それを理解するには、「水」が持つ特殊な性質が重要になってきます。
水は、水素原子2つと酸素原子1つから成る、H2Oで表される分子です。液体の水や水溶液では、一部のH2Oが、水素イオン(H+)と水酸化物イオン(OH-)に電離しています。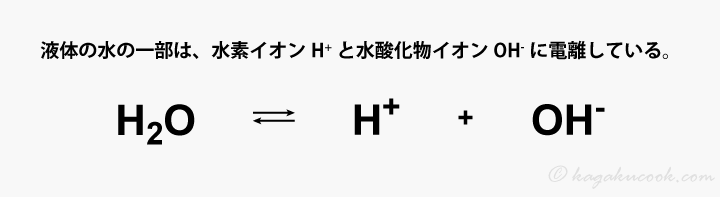 このH+やOH-こそが、水溶液に、酸性や塩基性(アルカリ性)といった性質をもたらす要因です。H+とOH-の濃度のバランスが、液性を決めます。
このH+やOH-こそが、水溶液に、酸性や塩基性(アルカリ性)といった性質をもたらす要因です。H+とOH-の濃度のバランスが、液性を決めます。
中性の場合、H+とOH-は、どちらも同じ濃度です。しかし、酸性水溶液中ではH+の方が多く、塩基性水溶液中ではOH-の方が多く存在します。
水に溶かすと水素イオン(H+)を放出し、水溶液が酸性になる物質は「酸」と呼ばれます。一方、水酸化物イオン(OH-)を放出したり、酸からH+を受け取ったりする物質は「塩基」と呼ばれ、その水溶液は塩基性です。
酸と塩基が水溶液で混ざると「中和反応」が起こり、塩が生じます(多くの場合、同時に水も生成)。
例えば、塩酸と水酸化ナトリウム水溶液を混ぜると中和が起こり、塩である塩化ナトリウム(NaCl)と水が生成します。
塩酸は、塩化水素(HCl)の水溶液のことです。
- 例:塩化水素と水酸化ナトリウムの中和の化学反応式
- HCl + NaOH → NaCl + H2O
重曹とクエン酸を混ぜる反応の化学反応式
下図は、重曹とクエン酸の化学反応式です。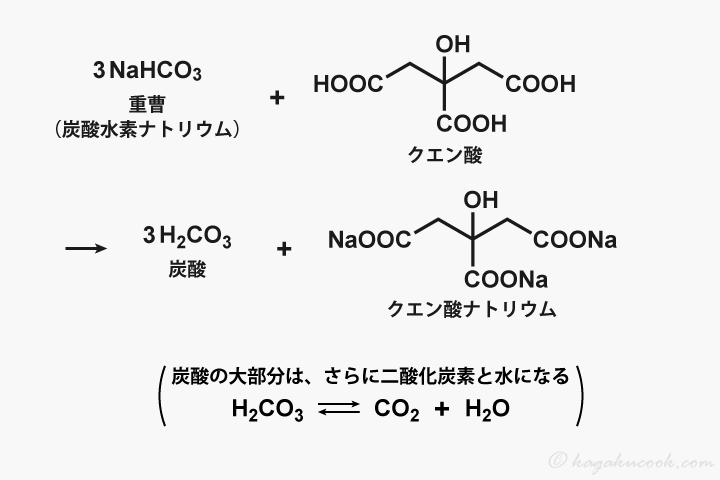
この化学反応式から、様々なことが読み取れます。「クエン酸の変化」「重曹の変化」「重曹とクエン酸が反応する比率」の3つのトピックに分けて、順に説明します。
クエン酸から弱塩基性を示す塩が生成
まずは、クエン酸の変化に着目して解説します。
クエン酸は、名前のとおり酸です。下記の化学式では、酸として働く(H+を放出する)部分の水素を赤く塗っています。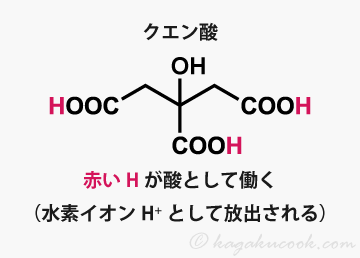
クエン酸は、重曹にH+を渡して、代わりにナトリウムイオンを受け取ります。生成するのは、塩であるクエン酸ナトリウムです。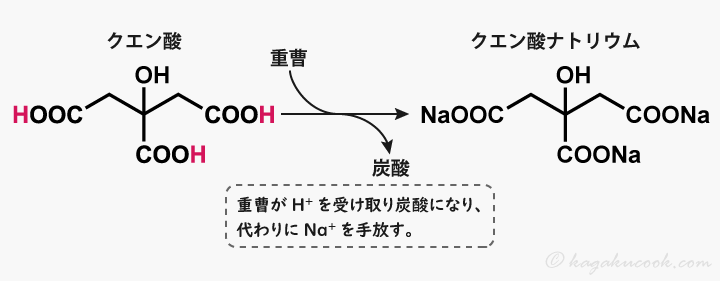
クエン酸ナトリウム(クエン酸三ナトリウム)は、酸としての性質はなく、水溶液は弱塩基性を示します。
水に重曹とクエン酸を混ぜるレシピで作った自家製炭酸水の中には、このクエン酸ナトリウムが含まれます。クエン酸ナトリウムにより食味が悪かったり、塩分が含まれていたりすることは、市販の炭酸水との大きな違いです。
味覚の観点では、クエン酸に強烈な酸味がある一方、クエン酸ナトリウムは酸ではないため酸味を持ちません。
筆者は実際に少量のクエン酸ナトリウム粉末を味わってみた経験がありますが、強い味はなく、少しだけ塩味を感じました。また、後味がよいとはいえず、わずかな後味の悪さ(苦味に近い感覚)がありました。
実際のところ、重曹とクエン酸から副生するクエン酸ナトリウムは、炭酸水を「まずく」する原因でもあります。
- 関連記事
- クエン酸の化学式・構造式や性質を詳しく解説 - カガクなキッチン
クエン酸の化学式や性質について解説しています。
重曹に酸を加えると「弱酸の遊離」が起こり炭酸が発生
次に、重曹の変化に着目して炭酸水ができる理由を解説しますが、その前に「二酸化炭素」と「炭酸」について知る必要があります。
二酸化炭素(CO2)は、近年では空気中に約0.041%含まれる、有機物の燃焼や動物の呼吸などに伴い発生する気体です。
このCO2を水に溶かすと、炭酸水になります。市販の炭酸水は、気体のCO2を、高い圧力のもと水に溶かしたものです。
水に溶けたCO2のうち、ごく一部は、水分子と反応して炭酸 (H2CO3)という分子になっています。炭酸は、非常に弱いながらも酸としての性質を持つので、炭酸水は酸性です。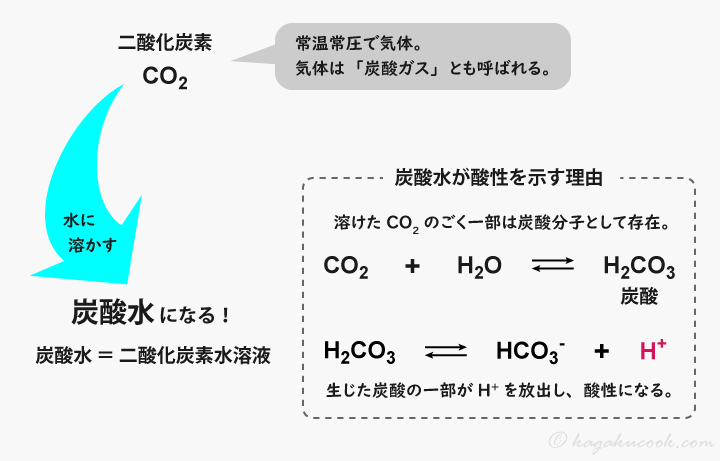
ちなみに、二酸化炭素ガス(気体のCO2)のことを「炭酸ガス」と呼びますが、これは炭酸(H2CO3)のことではありません。炭酸は、水溶液中にのみ存在する分子です。混同しないよう注意を要します。
重曹は、炭酸の塩です。重曹の化学的な名称は「炭酸水素ナトリウム」であり、化学式はNaHCO3です。重曹を水に溶かすと、ナトリウムイオンNa+と炭酸水素イオンHCO3-に電離して溶けます。
この炭酸水素イオンこそ、クエン酸との反応で、炭酸(H2CO3)を発生させる原料となる化学種です。
炭酸水素イオンは、(クエン酸などの)炭酸より強い酸からH+を受け取ります。そして、反応相手の酸が塩になる代わりに、炭酸が遊離します。「弱酸の遊離」と呼ばれる形式の反応です。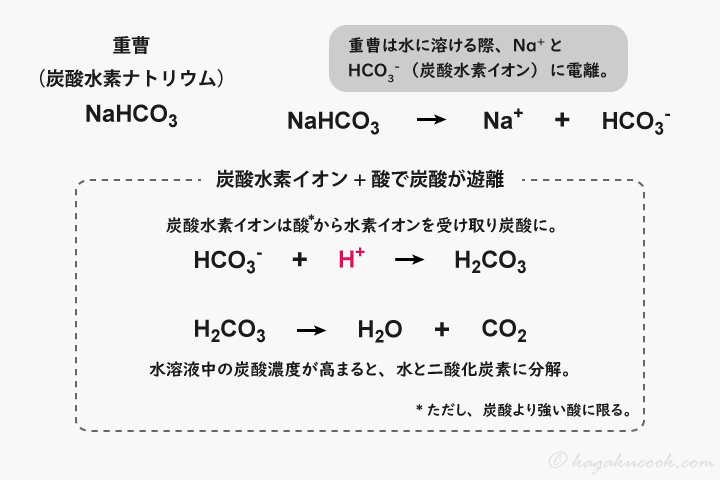
炭酸水ができる原理として「重曹とクエン酸を水に溶かすと二酸化炭素(炭酸ガス)が発生して水に溶け込み炭酸水になる」と説明されることも多いですが、あまり的を射た説明ではありません。
実際には、重曹とクエン酸を反応させた場合、水溶液中で炭酸(H2CO3)が生成します。この時点で、すでに炭酸水になっていると見なせるでしょう。
そして、水溶液中の炭酸と二酸化炭素の平衡(濃度のバランス)は、大きく二酸化炭素側に偏っています。水に溶けられる二酸化炭素濃度には上限があり、溶けきれなくなった二酸化炭素は、発泡して逃げていくのです。
つまり、発生した炭酸ガスが溶け込み炭酸水ができるというより、水溶液が(局所的に)炭酸水になった後、溶けきれなくなった溶存二酸化炭素が炭酸ガスとなって発泡しています。
- 関連記事
- 炭酸水素ナトリウム(重曹)の化学式NaHCO3の意味を丁寧に解説 - カガクなキッチン
重曹の化学式や性質について解説しています。
重曹とクエン酸は3:1の物質量比(モル比)で反応
重曹とクエン酸は、3:1の物質量比で反応します。クエン酸は3個のH+を放出できるのに対して、重曹から生じる炭酸水素イオンは1個のH+しか受け取れません。
そのため、ぴったり反応させるには、クエン酸の3倍の物質量(モル数)の重曹を要します。
これを質量や重さの比に換算するには、物質量(モル)の計算が必要です。本ページの計算ツールを使えば、誰でも簡単に混合量の計算ができるので、ぜひ活用してください。
まとめ
クエン酸と重曹を水溶液中で反応させると、気体が発生して発泡します。これは、「弱酸の遊離」と呼ばれる形式の化学反応により炭酸分子が生じて、水に溶けきれなかった分が二酸化炭素となって気化するためです。
この反応では、炭酸だけでなく、塩であるクエン酸ナトリウムも生成します。
化学反応は決まった比で起こるので、過不足なくぴったり反応させるには、化学的な計算値を基に、重曹とクエン酸の重さを量り取ることが必要です。


