クエン酸ナトリウムとは?pH・化学式・性質まとめ
当サイトには広告を掲載しています

クエン酸ナトリウムは、クエン酸のナトリウム塩です。その水溶液は、pHが8.6~8.7程度の弱塩基性(弱アルカリ性)を示します。
この記事では、クエン酸ナトリウム水溶液のpHを測定し、濃度とpHの一覧表を掲載しています。化学の専門知識を持つ筆者が、一般の方に向けて簡単に、クエン酸ナトリウムとはどんな物質かも解説します。
クエン酸ナトリウム水溶液のpHは?
クエン酸ナトリウムは、弱塩基性(弱アルカリ性)の物質です。いくつかの濃度でクエン酸ナトリウム水溶液を調製し、pHを測定した結果を下表にまとめます。
| クエン酸ナトリウム濃度 | pH |
|---|---|
| 20% | 8.71 |
| 5% | 8.67 |
| 1% | 8.65 |
| 0.1% | 8.02 |
クエン酸ナトリウム水溶液のpHは8.6~8.7程度です。ただし、1%を大きく下回れば、より低めのpHを示します。
クエン酸ナトリウム水溶液は、少なくとも1%以上の濃度があれば、濃度が上昇しても、pHの変化はわずかです。こうした性質は、弱酸と強塩基との塩では典型的です。
pH(ピーエイチ)とは、水溶液の酸性~中性~アルカリ性といった液性を数値化した指標です。ちょうど中性では、pHが7になります。7より小さいと酸性であり、大きいとアルカリ性を示します。

クエン酸ナトリウムとはどんな物質か解説!
クエン酸ナトリウムは、ナトリウムのアルカリ塩でクエン酸を中和すると生じる、クエン酸のナトリウム塩です。(クエン酸ナトリウムのように、酸とアルカリの中和反応により生じるような物質を「塩」と呼びます。)
ナトリウムのアルカリ塩とは、水酸化ナトリウム(苛性ソーダ)や炭酸ナトリウム、炭酸水素ナトリウムなどが該当します。
クエン酸ナトリウムの化学式
クエン酸はカルボン酸であり、カルボキシ基(-COOH) を持ちます。このカルボキシ基が、水中ではいくらかの割合で水素イオン(H+)を手放すため、クエン酸水溶液は酸性なのです。
クエン酸はカルボキシ基が3つある、3価のカルボン酸です。このため、分子内の3つの部分で塩基(アルカリ)と反応します。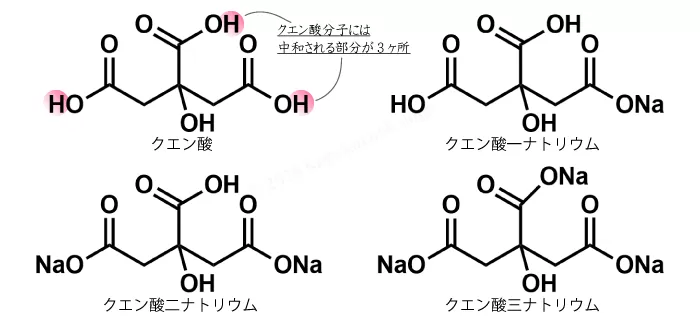 3つのカルボキシ基のうち、いくつがナトリウムのアルカリ塩と反応しているかの違いで、クエン酸一ナトリウム、クエン酸二ナトリウム、クエン酸三ナトリウムの3種類があります。
3つのカルボキシ基のうち、いくつがナトリウムのアルカリ塩と反応しているかの違いで、クエン酸一ナトリウム、クエン酸二ナトリウム、クエン酸三ナトリウムの3種類があります。
「クエン酸三ナトリウム」のことを指して、単に「クエン酸ナトリウム」と言う場合も多々あります。
クエン酸とクエン酸ナトリウムの違い
クエン酸は、名前のとおり酸性の物質です。濃厚な水溶液はpH1程度の強めの酸性を示し、1%水溶液でもpHは2.1程度です。
- 関連記事
- クエン酸のpH値はいくつ?水溶液の濃度別に実測値を公開!
クエン酸水溶液のpH実測値を公開した記事です。
クエン酸水溶液が酸性であるのに対し、クエン酸ナトリウム水溶液は弱塩基性(弱アルカリ性)です。

無水クエン酸、およびクエン酸三ナトリウム二水和物を使用して撮影。

また、食品成分として見た場合、両者の味は全く別物です。クエン酸は強い酸味を持ちますが、ナトリウム塩であるクエン酸三ナトリウムは、わずかに塩味を持っています。
まとめ
一般家庭では、クエン酸ナトリウムという物質そのものを扱う機会はほとんどありませんが、食品添加物などとしては非常によく用いられている物質です。
クエン酸の水溶液は酸性ですが、クエン酸三ナトリウムの水溶液は弱アルカリ性です。味の点でも、クエン酸三ナトリウムは酸味を持っていません。
このように、クエン酸と、クエン酸のナトリウム塩では、性質も大きく異なります。似たような関係は他の弱酸、例えば酢酸と酢酸ナトリウムなどでも成り立ちます。